Систему CRISPR-CAS9 удалось заснять в действии
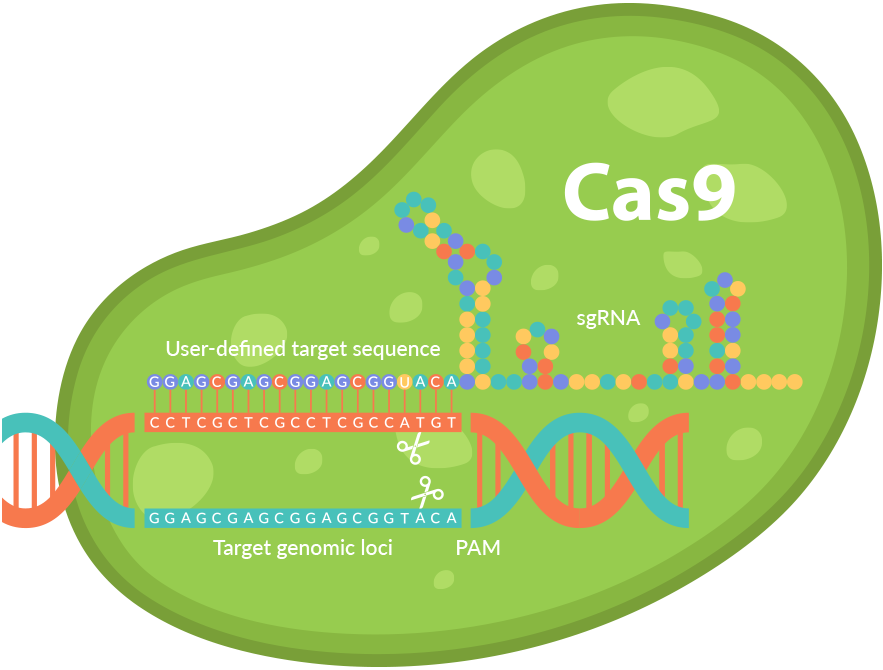
Несмотря на уже более чем десятилетнюю историю изучения системы CRISPR-Cas и применения ее для редактирования генома, до сих пор никто не наблюдал ее за работой. Японские ученые устранили этот пробел и первыми в мире получили видео этого процесса, используя высокоскоростной атомно-силовой микроскоп. При этом выяснилось, что элементы системы связываются с молекулами ДНК не так, как считалось ранее: они не ползают по этим молекулам в поисках нужного места, а находят его при помощи трехмерной диффузии.
Система CRISPR-Cas9, которая используется для направленного редактирования генома, завоевала большую популярность среди ученых. Количество статей, в которых упоминается эта система, стремительно растет с каждым годом (начиная с нескольких статей в 2011 году и заканчивая более чем двумя тысячами статей в 2017 году).
Открытая почти 30 лет назад, более 20 лет эта система представляла интерес только для молекулярных биологов, которые пытались понять свойства этого уникального защитного механизма. В 2012 году был выявлен потенциал систем CRISPR-Cas9 как инструмента для редактирования генома, способного инициировать целенаправленные генетические модификации практически в любом организме. В последующие годы с помощью этого метода ученым удалось, например, избавить мышей от генетических заболеваний и даже отредактировать геномы эмбриона и взрослого человека.
Несмотря на существенные успехи, по сей день не было ни одного прямого наблюдения функционирования этой системы. Этот пробел удалось устранить группе японских ученых во главе с Микихиро Шибатой (Mikihiro Shibata) при помощи высокоскоростного атомно-силового микроскопа (HS-AFM), который позволяет получать изображения молекул и даже отдельных атомов. Статья об исследовании опубликована в журнале Nature Communications.
С помощью HS-AFM-визуализации можно выявлять динамику белков с фантастической детализацией. Например, ранее ученым, среди которых были и некоторые авторы обсуждаемой работы, удалось зафиксировать фотоиндуцированные конформационные изменения в молекуле бактериородопсина(M. Shibata et al., 2010. High-speed atomic force microscopy shows dynamic molecular processes in photoactivated bacteriorhodopsin) и пронаблюдать за молекулой миозина, прогуливающейся по актиновой нити (N. Kodera et al., 2010. Video imaging of walking myosin V by high-speed atomic force microscopy).
Также ученым удалось опровергнуть теорию о том, как именно комплекс Cas9-РНК связывается с необходимым участком на молекуле ДНК: ранее считалось, что белок, связанный с РНК, «скользит» по ДНК в поисках комплементарного участка. Для этого исследователи использовали подложку с билипидным слоем, чтобы минимизировать взаимодействие между слюдой и белком, которое может помешать свободной диффузии комплекса. Оказалось, что Cas9 без направляющей РНК связывается с молекулой ДНК и просто скользит по ней. А вот когда у белка есть РНК, комплементарная нужному участку, комплекс не скользит, а напрямую связывается с мишенью. Видимо, наличие направляющей РНК мешает комплексу Cas9-РНК «оседлать» ДНК, чтобы скользить по ней. Так что связывание происходит за счет трехмерной диффузии: комплексы плавают в растворе, а если им повезет оказаться рядом с нужным участком ДНК, то они с ним связываются.
Подробнее: https://elementy.ru/novosti_nauki/433160/Sistemu_CRISPR_CAS9_udalos_zasn...
